Libri personalizzati
Scuole superiori
Meccanica
Termodinamica
Oscillazioni e onde
Elettromagnetismo
Libri degli insegnanti




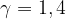 ) fin quando il suo volume arriva a 0,05 mc.
) fin quando il suo volume arriva a 0,05 mc.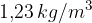 .
.


